
市場規模
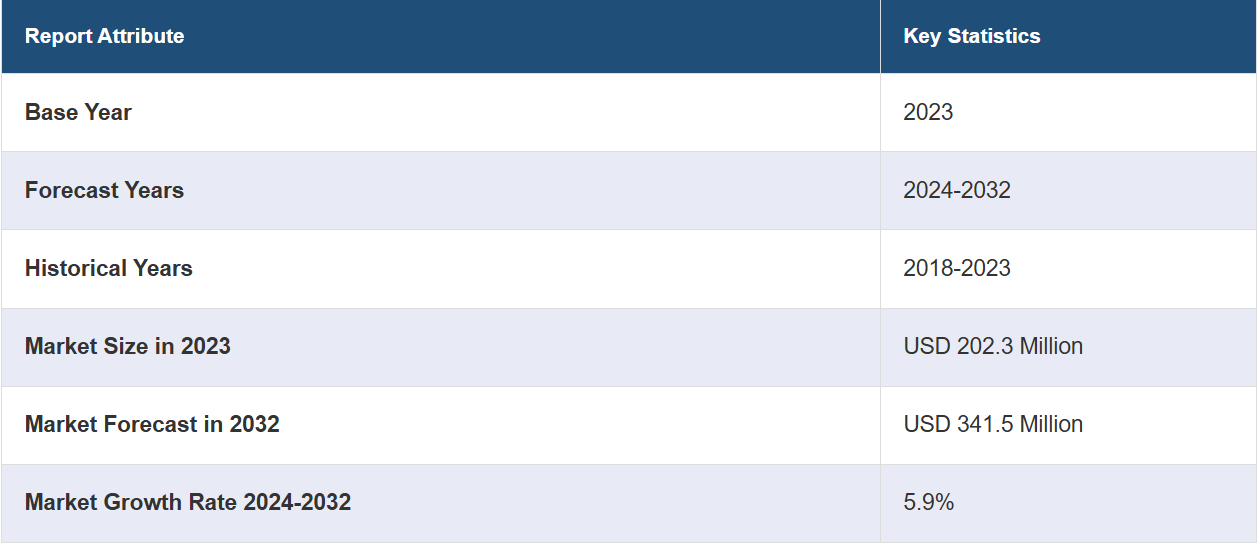
世界のファーマコビジランス&医薬品安全性ソフトウェア市場規模は、2023年には2億2300万米ドルに達する見通しです。今後、IMARC Groupは、市場が2032年までに3億4,150万米ドルに達すると予測しており、2024年から2032年の年間平均成長率(CAGR)は5.9%と予測しています。 大衆における慢性疾患の増加、医薬品の商業化に関する厳格な規制の実施、ソフトウェアの機能とユーザーフレンドリーなインターフェースの継続的な進歩は、市場を推進する主な要因のいくつかです。
ファーマコビジランス&医薬品安全性ソフトウェアとは、医薬品副作用(ADR)やその他の医薬品関連の安全性に関する懸念事項のモニタリング、分析、報告を合理化し、強化するために設計された専門のコンピュータプログラムを指します。これらのソフトウェアシステムは、医薬品の安全かつ効果的な使用を確保することを目的とするファーマコビジランス分野において重要な役割を果たしています。これらのソフトウェアソリューションにより、製薬会社、規制当局、医療従事者は、医薬品の安全性に関する大量のデータを効率的に収集、管理、分析することが可能になります。また、潜在的なリスクやパターンを検出し、迅速な介入とリスク軽減戦略を可能にします。
ファーマコビジランス&医薬品安全性ソフトウェア市場は、臨床研究およびアウトソーシング企業によるこれらのソフトウェアソリューションの採用増加によって牽引されています。これらの組織は、開発中の医薬品および市販後調査における安全性と有効性を確保するための強固なファーマコビジランスシステムの重要性を認識しています。さらに、慢性疾患の増加も市場の成長に寄与しています。長期投薬を必要とする患者の数が増加するにつれ、効果的な医薬品安全性の監視と管理の必要性も高まっています。これとは別に、世界各国の政府が医薬品の商業化に厳しい規制を課しているため、医薬品安全性規制の複雑性が増しており、これが需要をさらに促進しています。さらに、最先端技術の利用により、ファーマコビジランス&医薬品安全性ソフトウェアの導入が容易になっています。さらに、ソフトウェアの機能とユーザーフレンドリーなインターフェースの継続的な進歩により、組織がこれらのソリューションを既存のワークフローに実装し、統合することが容易になり、市場に好影響を与えています。
ファーマコビジランス&医薬品安全性ソフトウェア市場の動向/推進要因:
製薬業界の拡大
製薬業界の発展は、世界的なファーマコビジランス(PV)および医薬品安全性ソフトウェア市場に大きな影響を与えています。製薬業界が拡大するにつれ、新薬や治療法の開発も増加しています。これにより、有害事象の監視、分析、管理を行うPVおよび医薬品安全性ソフトウェアの必要性が高まり、このソフトウェアに対する需要も増加しています。さらに、製薬業界の拡大によりデータ量と複雑性が増大し、データの管理と分析には高度なソフトウェアが必要となっています。このため、PVおよび医薬品安全性ソフトウェアでは、このような複雑なデータセットを効果的に処理するために、AIと機械学習の開発と導入が進んでいます。また、ファーマコビジランス&医薬品安全性ソフトウェアは、これらのリスクの管理に役立ち、リスク管理のニーズの高まりがこの市場の需要を牽引しています。
増加する医薬品副作用の発生率
医薬品副作用(ADR)の発生件数の増加は、世界的なファーマコビジランス&医薬品安全性ソフトウェア市場に大きな影響を与えています。 報告される医薬品副作用の件数の増加により、市場に出回る医薬品の安全性と有効性を確保するための強固なファーマコビジランスシステムおよびソフトウェアソリューションに対するニーズが高まっています。 医薬品副作用は患者の健康と幸福に深刻な影響を及ぼし、入院や医療費の増加、さらには死亡につながることもあります。そのため、世界中の規制当局は、製薬会社が副作用を効果的に監視・報告するための厳格なガイドラインや規制を導入しています。これに伴い、世界的なファーマコビジランス&医薬品安全性ソフトウェア市場は、副作用の発生件数の増加に直接対応する形で著しい成長を遂げています。これらのソフトウェアソリューションを提供する企業は、大量の有害事象データを効率的に処理できる高度なツールや機能を提供するために絶え間なく革新を続けているためです。
増加する医療費
医療費が世界的に増加し続ける中、患者の安全性の最適化と医療の質全体の改善がますます重視されるようになっています。 ファーマコビジランス&医薬品安全性ソフトウェアは、医薬品副作用(ADR)やその他の医薬品関連問題の効果的なモニタリング、評価、管理を確実に実施することで、これらの目標の達成に重要な役割を果たします。医療費の増加に伴い、患者の安全性に対する注目が高まっています。 ファーマコビジランスソフトウェアは、医療機関や規制当局に副作用を監視し、防止するためのツールを提供することで、薬物関連の被害に関連する経済的負担を軽減します。 さらに、医療費の増加に伴い、リソースの最適化が求められています。 さらに、ファーマコビジランスソフトウェアは、有害事象データの効率的な管理を可能にし、報告と分析のプロセスを合理化します。
ファーマコビジランス&医薬品安全性ソフトウェア業界の区分:
IMARC Groupは、世界のファーマコビジランス&医薬品安全性ソフトウェア市場レポートの各セグメントにおける主要な傾向の分析を提供しています。また、2024年から2032年までの世界、地域、国レベルでの予測も行っています。当社のレポートでは、機能、提供形態、エンドユーザーに基づいて市場を分類しています。
機能別内訳:
有害事象報告ソフトウェア
医薬品安全性監査ソフトウェア
問題追跡ソフトウェア
完全統合ソフトウェア
有害事象報告ソフトウェアが市場を独占
本レポートでは、機能別に市場の詳細な内訳と分析を提供しています。これには、有害事象報告ソフトウェア、医薬品安全性監査ソフトウェア、問題追跡ソフトウェア、完全統合ソフトウェアが含まれます。レポートによると、有害事象報告ソフトウェアが最大のセグメントを占めています。
有害事象報告ソフトウェアは、ヘルスケアおよび製薬業界における規制順守の重要な側面であるため、市場を独占しています。このソフトウェアは強力なデータ管理機能を備えており、有害事象データの効率的な収集、整理、分析を可能にします。特定の製品や治療法に関連するパターン、傾向、潜在的な安全性の問題を特定することができます。このデータ主導のアプローチは、製薬会社、医療従事者、規制当局が製品の安全性とリスク軽減戦略に関する情報に基づいた意思決定を行うのに役立ちます。さらに、これらの事象の把握と報告に体系化された標準化されたアプローチを提供し、規制要件へのコンプライアンスを確実にします。 医療従事者、医薬品安全性の専門家、有害事象報告に関わるその他の利害関係者に対して、一元化されたプラットフォームを提供します。 また、このソフトウェアは、大量の有害事象データを処理できる拡張性があり、報告要件の多い組織でもその有効性を確保できます。
配信モード別内訳:
オンプレミス
クラウドベース
オンプレミス型配信は市場で最大のシェアを占めている
配信形態に基づく市場の詳細な内訳と分析も、このレポートで提供されています。これにはオンプレミス型とクラウド型が含まれます。レポートによると、オンプレミス型が最大の市場シェアを占めています。
オンプレミス型は、企業がデータに対してより高度な管理とセキュリティを確保できるため、市場で最大のシェアを占めています。 また、カスタマイズや既存システムとの統合の面でも高い柔軟性を備えています。 企業は、自社の要件に合わせてソフトウェアをカスタマイズし、他のオンプレミス型アプリケーションやインフラとシームレスに統合することができます。 このレベルのカスタマイズと統合は、複雑なIT環境や独自のビジネスプロセスを持つ企業にとって有益です。この導入により、機密データを自国内に留めることでデータの主権を維持することができます。さらに、オンプレミスソフトウェアの普及により、ネットワークの遅延やインターネット接続への依存に関連する潜在的なパフォーマンスの問題を排除することができます。また、コンプライアンスを維持し、規制基準を満たすこともより容易になります。
エンドユーザー別:
製薬およびバイオテクノロジー企業
医薬品開発業務受託機関
ビジネスプロセスアウトソーシング企業
その他
市場で最大のシェアを占めているのは医薬品開発業務受託機関
エンドユーザー別の市場の詳細な内訳と分析も報告書に記載されています。これには、製薬会社およびバイオテクノロジー企業、医薬品開発業務受託機関、ビジネスプロセスアウトソーシング企業、その他が含まれます。報告書によると、医薬品開発業務受託機関が最大の市場シェアを占めています。
CROは重要な地位を占めており、市場の製品やサービスにおける主要なユーザーとなっています。 CROは総合的な研究サービスの提供を専門としており、製薬会社やバイオテクノロジー企業が研究開発活動のさまざまな側面をアウトソーシングすることを可能にしています。 このアウトソーシングモデルには、専門知識へのアクセス、運用コストの削減、試験実施の効率化など、数多くの利点があります。同社は、業界のベストプラクティス、規制要件、新たなトレンドに関する深い知識を提供しており、複雑な研究プロセスをナビゲートし、成果を達成するための信頼できるパートナーを求める企業にとって魅力的な選択肢となっています。また、プロジェクトの要件に応じてリソースとインフラを拡張する能力も備えており、小規模な研究から大規模な国際共同治験までサポートが可能です。リスク管理、データの完全性、コンプライアンスに関する専門知識を提供しており、企業が複雑な規制環境をナビゲートし、潜在的な落とし穴を軽減する手助けをしています。
地域別内訳:
北米
米国
カナダ
アジア太平洋地域
中国
日本
インド
韓国
オーストラリア
インドネシア
その他
ヨーロッパ
ドイツ
フランス
英国
イタリア
スペイン
ロシア
その他
中南米
ブラジル
メキシコ
その他
中東およびアフリカ
北米が圧倒的な優位性を示しており、ファーマコビジランス&医薬品安全性ソフトウェア市場で最大のシェアを占めている
また、このレポートでは、北米(米国およびカナダ)、アジア太平洋(中国、日本、インド、韓国、オーストラリア、インドネシアなど)、ヨーロッパ(ドイツ、フランス、英国、イタリア、スペイン、ロシアなど)、中南米(ブラジル、メキシコなど)、中東およびアフリカといった主要な地域市場の包括的な分析も行っています。レポートによると、北米が最大の市場シェアを占めています。
北米には、創薬、開発、商品化に携わる多数の企業を抱える、強固で確立された製薬業界があります。この地域は、ヘルスケアや情報技術の進歩を含む技術革新の最前線に位置しています。この地域には強固なITインフラがあり、研究開発に適した投資環境が整っており、デジタルソリューションの採用に重点的に取り組んでいます。北米の製薬会社や研究機関は、学術機関、医療提供者、テクノロジー企業と連携し、ファーマコビジランスや医薬品安全性の革新を推進することが多い。こうした連携により、最先端のソフトウェアソリューションの開発と採用が促進され、北米の市場における優位性がさらに高まる。さらに、この地域では医薬品安全性に対する規制要件が厳しく、ファーマコビジランスが北米市場全体を牽引するもう一つの重要な要因となっている。
競合状況
市場のトップ企業は、高度なファーマコビジランス&医薬品安全性ソフトウェアソリューションを開発するための研究開発活動に投資しています。これらのソフトウェアプラットフォームは、医薬品および医療介入に関連する有害事象、安全性データ、その他の関連情報を取得、処理、分析、報告するように設計されています。さまざまな企業が、製薬会社、CRO、医療機関の独自のニーズに合わせてカスタマイズできる柔軟性と拡張性のあるソフトウェアプラットフォームを提供しています。さらに、各社は人工知能(AI)や機械学習(ML)などの高度なデータ分析技術を活用し、大量の安全性データを分析して潜在的な安全性シグナルを特定しています。これらの分析機能は、有害事象の早期発見、シグナル管理、リスク評価、トレンド分析に役立ちます。
このレポートでは、市場における競争環境の包括的な分析を提供しています。また、すべての主要企業の詳しいプロフィールも提供されています。市場における主要企業の一部は以下の通りです。
Ab Cube
Anju Software Inc.
ArisGlobal LLC
Cognizant
Ennov Solutions Inc.
Extedo GmbH
Max Application
Oracle Corporation
Sarjen Systems Pvt Ltd
Sparta Systems Inc. (Honeywell International Inc.)
Tata Consultancy Services Limited
United BioSource LLC
Wipro Limited
最近の動向:
2023年2月、Aris Globalは治験段階の企業向けに特化した規制情報管理ソリューションを発表しました。この新製品は、新興のライフサイエンス企業や医療機器企業に最適です。次の臨床または規制上のマイルストーンを達成するために必要な機能に重点的に取り組むように設計されています。
2022年6月、Tata Consultancy Servicesは、顧客がサブスクリプションファーストのビジネスモデルを構築し、インテリジェントなサービス機能を備えた成果ベースのソリューションを提供できるよう支援する「TCS Servitization Engine on Oracle Cloud」を発表しました。このエンジンは、製品、サービス、サポート、セルフサービス、ナレッジベースを組み合わせた業界向けパッケージを提供しており、企業はこれを活用して、堅牢な顧客向けフロントエンドソリューションとともに、自社の主力製品に付加価値を加えることができます。
2022年10月、CognizantはQualcommとの提携を発表し、デジタル変革のための5Gエクスペリエンスセンターを立ち上げました。この提携により、自動運転、ロボットオートメーション、合成生物学、仮想現実、スマート製造などのサービスを、超信頼性、低レイテンシ、セキュア、スケーラブルな方法で提供できるようになります。
【目次】
1 序文
2 範囲と方法論
2.1 本調査の目的
2.2 利害関係者
2.3 データソース
2.3.1 一次ソース
2.3.2 二次ソース
2.4 市場推定
2.4.1 ボトムアップアプローチ
2.4.2 トップダウンアプローチ
2.5 予測方法論
3 エグゼクティブサマリー
4 はじめに
4.1 概要
4.2 主な業界動向
5 グローバルファーマコビジランス&医薬品安全性ソフトウェア市場
5.1 市場概要
5.2 市場実績
5.3 COVID-19の影響
5.4 市場予測
6 機能別市場内訳
6.1 有害事象報告ソフトウェア
6.1.1 市場動向
6.1.2 市場予測
6.2 医薬品安全性監査ソフトウェア
6.2.1 市場動向
6.2.2 市場予測
6.3 課題追跡ソフトウェア
6.3.1 市場動向
6.3.2 市場予測
6.4 完全統合ソフトウェア
6.4.1 市場動向
6.4.2 市場予測
7 デリバリーモード別市場
7.1 オンプレミス
7.1.1 市場動向
7.1.2 市場予測
7.2 クラウドベース
7.2.1 市場動向
7.2.2 市場予測
8 エンドユーザー別市場
8.1 製薬およびバイオテクノロジー企業
8.1.1 市場動向
8.1.2 市場予測
8.2 医薬品開発業務受託機関
8.2.1 市場動向
8.2.2 市場予測
8.3 ビジネスプロセスアウトソーシング企業
8.3.1 市場動向
8.3.2 市場予測
8.4 その他
8.4.1 市場動向
8.4.2 市場予測
9 地域別市場規模
9.1 北米
9.1.1 米国
9.1.1.1 市場動向
9.1.1.2 市場予測
9.1.2 カナダ
9.1.2.1 市場動向
9.1.2.2 市場予測
9.2 アジア太平洋地域
9.2.1 中国
9.2.1.1 市場動向
9.2.1.2 市場予測
9.2.2 日本
9.2.2.1 市場動向
9.2.2.2 市場予測
9.2.3 インド
9.2.3.1 市場動向
9.2.3.2 市場予測
9.2.4 韓国
9.2.4.1 市場動向
9.2.4.2 市場予測
9.2.5 オーストラリア
9.2.5.1 市場動向
9.2.5.2 市場予測
9.2.6 インドネシア
9.2.6.1 市場動向
9.2.6.2 市場予測
9.2.7 その他
9.2.7.1 市場動向
9.2.7.2 市場予測
9.3 欧州
9.3.1 ドイツ
9.3.1.1 市場動向
9.3.1.2 市場予測
9.3.2 フランス
9.3.2.1 市場動向
9.3.2.2 市場予測
9.3.3 英国
9.3.3.1 市場動向
9.3.3.2 市場予測
9.3.4 イタリア
9.3.4.1 市場動向
9.3.4.2 市場予測
9.3.5 スペイン
9.3.5.1 市場動向
9.3.5.2 市場予測
9.3.6 ロシア
9.3.6.1 市場動向
9.3.6.2 市場予測
9.3.7 その他
9.3.7.1 市場動向
9.3.7.2 市場予測
9.4 ラテンアメリカ
9.4.1 ブラジル
9.4.1.1 市場動向
9.4.1.2 市場予測
9.4.2 メキシコ
9.4.2.1 市場動向
9.4.2.2 市場予測
9.4.3 その他
9.4.3.1 市場動向
9.4.3.2 市場予測
9.5 中東およびアフリカ
9.5.1 市場動向
9.5.2 国別の市場内訳
9.5.3 市場予測
…
【お問い合わせ・ご購入サイト】
資料コード:SR112024A5030

