
市場規模
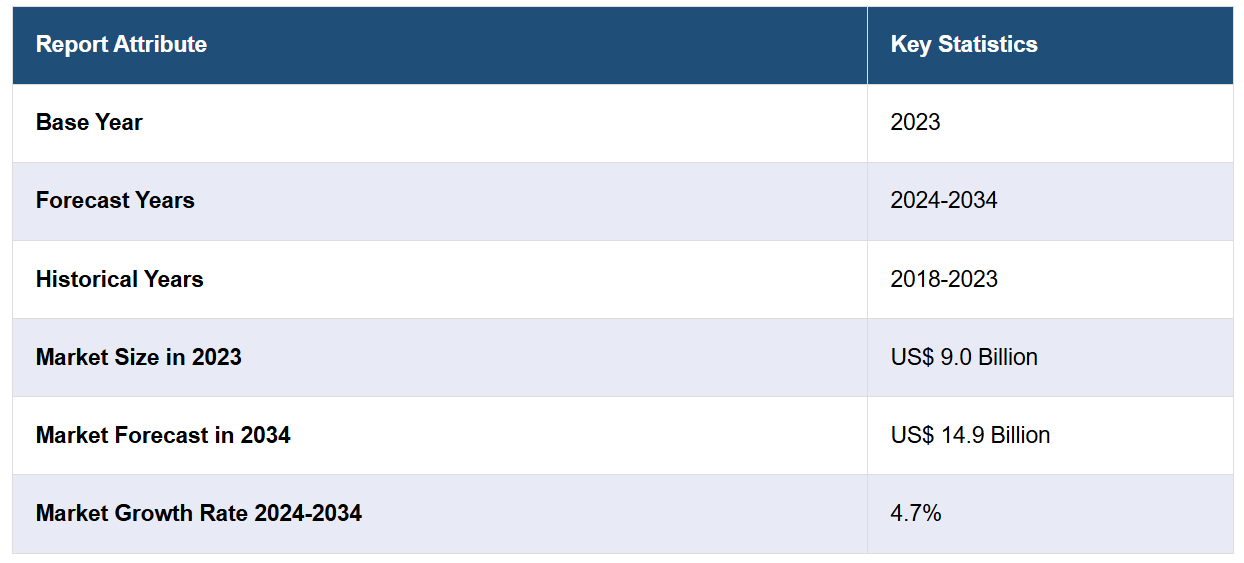
クロストリジウム・ディフィシル感染症の7大市場は、2023年に90億米ドルに達しました。IMARC Groupは、7MMが2034年までに149億米ドルに達し、2024年から2034年の年間平均成長率(CAGR)は4.7%になると予測しています。
クロストリジウム・ディフィシル感染症市場は、IMARCの最新レポート「クロストリジウム・ディフィシル感染症市場:疫学、業界動向、シェア、規模、成長、機会、予測 2024年~2034年」で包括的に分析されている。クロストリジウム・ディフィシル感染症(CDI)とは、病原性細菌であるクロストリジウム・ディフィシル(通称C. difficile)による細菌感染症を指す。この細菌は大腸に定着し、腸内細菌叢の正常なバランスを崩すことで、さまざまな胃腸症状を引き起こします。 CDIの症状は重症度によって異なり、水様性下痢、腹痛、発熱、食欲不振、吐き気などが現れることがあります。 重症例では、偽膜性大腸炎という大腸のより重度の炎症に進行し、生命を脅かす合併症を引き起こすこともあります。CDIの診断には通常、いくつかの段階を踏みます。主な方法は、糞便サンプルを検査して、C. difficile毒素または細菌そのものの存在を調べる方法です。検査結果が陽性で、臨床症状が伴う場合、感染の確認には十分であることがよくあります。さらに、医療従事者は大腸内視鏡検査またはS状結腸鏡検査を行い、炎症や偽膜の兆候がないか大腸を目視で検査することもあります。
広域スペクトル抗生物質の使用が増加していることが、大腸内の有益な細菌のバランスを崩し、クロストリジウム・ディフィシルが過剰増殖して毒素を産生し、感染を引き起こす原因となっています。これが、クロストリジウム・ディフィシル感染症市場を主に牽引しています。これに加えて、バンコマイシンやフィダキソマイシンなどの有効な薬剤に対する需要の高まり、および健康な腸内微生物叢を回復させるための糞便微生物移植(FMT)の利用が新たに登場していることも、市場に明るい見通しをもたらしています。さらに、医療施設における感染管理対策や厳格な衛生プロトコルの広範な採用は、CDI感染の防止に重要な役割を果たしているため、市場の成長をさらに後押ししています。これとは別に、酵素免疫測定法(EIA)や核酸増幅検査(NAAT)などの迅速診断検査の適用が増加し、疾患の早期かつ正確な検出が可能になっていることも、成長を促すもう一つの重要な要因となっています。さらに、細菌の有害な作用を中和するのに役立つ細菌毒素を標的とするモノクローナル抗体などの革新的な治療法が普及しつつあることも、市場の成長を後押ししています。さらに、高リスク集団におけるCDI発生の予防を目的とした、クロストリジウム・ディフィシルに対する新規ワクチンの研究が進められていることも、予測期間中のクロストリジウム・ディフィシル感染症市場の成長を促進すると見込まれています。
IMARC Groupの最新レポートは、米国、EU4(ドイツ、スペイン、イタリア、フランス)、英国、日本におけるクロストリジウム・ディフィシル感染症市場を徹底的に分析しています。これには、治療方法、市場、開発中の薬剤、個々の治療法のシェア、7つの主要市場における市場実績、主要企業およびその薬剤の市場実績などが含まれます。また、本レポートでは、7つの主要市場における現在の患者数と将来の患者数も予測しています。本レポートによると、クロストリジウム・ディフィシル感染症の患者数が最も多いのは米国であり、また、その治療市場も最大となっています。さらに、現在の治療方法/アルゴリズム、市場の推進要因、課題、機会、償還シナリオ、未充足の医療ニーズなども報告されています。本報告書は、メーカー、投資家、事業戦略家、研究者、コンサルタント、およびクロストリジウム・ディフィシル感染症市場に何らかの利害関係を有する方、または何らかの形で同市場への参入を計画している方にとって必読の報告書です。
最近の動向:
2024年5月、Vedanta Biosciencesは、グローバル第3相RESTORATiVE303臨床試験において最初の患者への投与が実施されたと報告した。RESTORATiVE303試験では、再発性C. difficile感染症患者を対象にVE303の有効性と安全性を評価している。この試験は、米国食品医薬品局(FDA)に提出する生物製剤認可申請(BLA)の基礎となることを目的としている。
主なハイライト:
クロストリジウム・ディフィシルは、抗生物質関連下痢症の15~25%および抗生物質関連偽膜性大腸炎のほぼ全症例の原因となっています。
クロストリジウム・ディフィシル感染症の90%以上は、抗生物質治療後または治療中に発症します。
クロストリジウム・ディフィシルの無症候性保菌者は、病院環境を汚染する可能性があります。保菌者の割合は、健康な人ではおよそ3%、入院患者では20~30%、長期入院患者では50%です。
CDCは、クロストリジウム・ディフィシルが米国で毎年およそ50万件の疾患を引き起こしていると推定しています。
医療関連のクロストリジウム・ディフィシル感染症と診断された65歳以上の患者の11人に1人が、1か月以内に死亡しています。
薬剤:
ZINPLAVAは、クロストリジウム・ディフィシル毒素Bに結合するヒト型モノクローナル抗体です。クロストリジウム・ディフィシル感染症(CDI)の治療に抗菌薬を使用しており、再発リスクの高い1歳以上の成人および小児患者のCDI再発抑制に使用されます。
VE303は、クロストリジウム・ディフィシル感染症の再発を予防することを目的とした特定の細菌共同体で構成された、ファースト・イン・クラスの生菌生物製剤(LBP)候補です。これは、Vedanta社の製品エンジンを活用して合理的に選択された8つの菌株で構成されています。VE303は、純粋なクローン細菌細胞バンクから作られており、均一な粉末状の医薬品となり、成分が異なるドナー便に頼る必要がなくなります。
CP101は、単回の経口投与で微生物群全体を投与する試験段階のマイクロバイオーム治療薬であり、腸管準備の必要性を排除します。CP101は、多様な微生物群と、定着抵抗性に寄与すると考えられる重要な生理学的メカニズムを回復させることで、C. difficile感染症の再発を予防することを目的としています。
調査対象期間
基準年:2023年
歴史期間:2018年~2023年
市場予測:2024年~2034年
対象国
米国
ドイツ
フランス
英国
イタリア
スペイン
日本
各国における分析内容
過去の、現在の、および将来の疫学シナリオ
クロストリジウム・ディフィシル感染症市場の過去の、現在の、および将来のパフォーマンス
市場における各種治療カテゴリーの過去の、現在の、および将来のパフォーマンス
クロストリジウム・ディフィシル感染症市場における各種薬剤の売上
市場における償還シナリオ
市場内および開発中の薬剤
競合状況
本レポートでは、クロストリジウム・ディフィシル感染症の現行治療薬と後期開発段階にあるパイプライン薬剤の詳細な分析も提供しています。
市場で販売されている薬剤
薬剤概要
作用機序
規制状況
臨床試験結果
薬剤の普及状況と市場実績
後期開発段階にあるパイプライン薬剤
薬剤概要
作用機序
規制状況
臨床試験結果
薬剤の普及状況と市場実績
【目次】
1 序文
2 範囲と方法論
2.1 本調査の目的
2.2 利害関係者
2.3 データソース
2.3.1 一次ソース
2.3.2 二次ソース
2.4 市場推定
2.4.1 ボトムアップアプローチ
2.4.2 トップダウンアプローチ
2.5 予測方法論
3 エグゼクティブサマリー
4 クロストリジウム・ディフィシル感染症 – はじめに
4.1 概要
4.2 規制プロセス
4.3 疫学(2018~2023年)および予測(2024~2034年
4.4 市場概要(2018~2023年)および予測(2024~2034年
4.5 競合情報
5 クロストリジウム・ディフィシル感染症 – 疾患概要
5.1 はじめに
5.2 症状と診断
5.3 病態生理学
5.4 原因とリスク要因
5.5 治療
…
【お問い合わせ・ご購入サイト】
資料コード:SR112025A13281

